Категории
Сменить пароль!
Сброс пароля!


Вакцина против H. pylori могла бы стать основным средством профилактики хеликобактериоза и этиологически связанных заболеваний, однако текущие исследования в этой области сопряжены с большими трудностями.

Helicobacter pylori (H. pylori) — микроаэрофильная грамотрицательная жгутиковая изогнутая палочковидная бактерия, которой заражена половина населения планеты [1].
Россия — страна с высокой
распространенностью H. pylori
(около 90% населения) [2]
H. pylori является ключевым фактором развития ряда заболеваний желудочно-кишечного тракта, таких как хронический гастрит, язвенная болезнь и лимфома, ассоциированная со слизистой оболочкой (в частности, основным фактором риска развития рака желудка) [3].

Эффективность эрадикационной терапии в РФ — 59–79% [4]

Частота побочных реакций колеблется от 5 до 30% и в ряде случаев приводит пациента к решению прекратить лечение [6]. И присутствие H. pylori, и эрадикационная терапия способны привести к краткосрочным и долгосрочным клиническим последствиям [5].

Снижение эффективности схем эрадикации H. pylori, а также побочные эффекты на фоне лечения вызывают озабоченность специалистов и требуют усовершенствования терапии [5].
Вакцина — не фантастика,
а активно исследуемая стратегия


Первые опыты
Еще в 1984 году было показано, что повторная пероральная иммунизация холерным токсином индуцирует мукозальный иммунитет у грызунов [7].

В 1996 году Крайсс и др. ученые провели новаторское клиническое исследование и обнаружили, что, несмотря на пероральный прием рекомбинантной H. pylori уреазной вакцины, все добровольцы оставались инфицированными бактерией, что подчеркивало необходимость дальнейших исследований [9].
Почему вакцина до сих пор не создана?
Основные причины, по которым до сих пор не разработана вакцина от H. pylori
Новые надежды

В совокупности эти исследования указывают на потенциал новых вакцин и платформ для борьбы с инфекцией H. pylori. Однако необходимы исследования во всех направлениях, ведь прорыв может произойти не в виде вакцины, а благодаря комбинированным или альтернативным решениям.
А пока нет вакцины...
В отсутствие вакцины повышение эффективности эрадикационной терапии — приоритетная задача гастроэнтерологии.
Многочисленные исследования на животных и результаты доклинических испытаний показали, что лактобактерии могут помочь в профилактике
и лечении многочисленных заболеваний желудочно-кишечного тракта [15].
Было выявлено, что род Lactobacillus включает примерно 90 видов
с широким спектром биохимических и физиологических свойств [16]
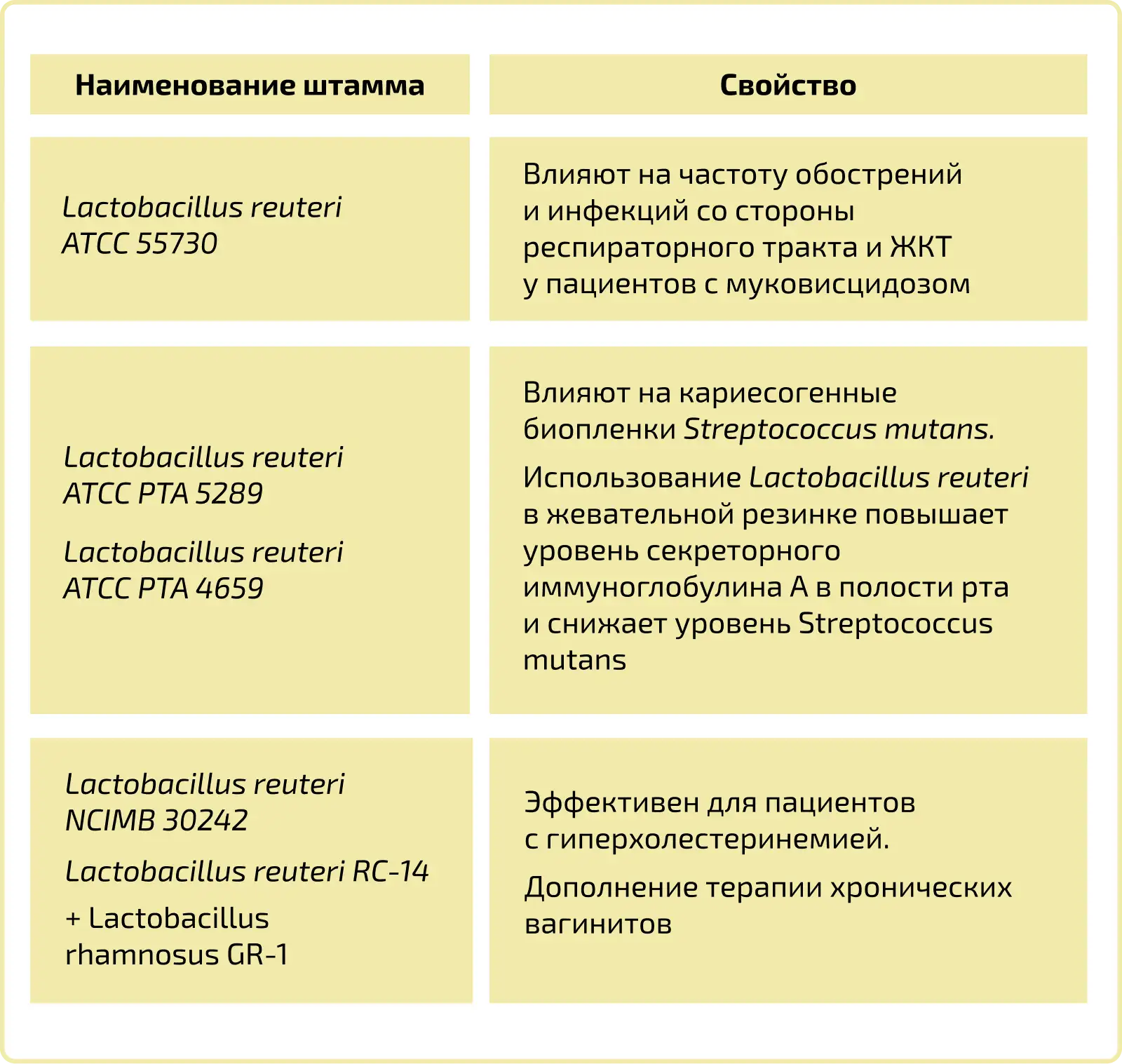
Наиболее изученные штаммы Lactobacillus reuteri и их
влияние при различной патологии [16]
В результате изучения более чем 700 штаммов L. reuteri был выделен уникальный штамм Lactobacillus reuteri DSM 17648 [17].
Доказана уникальная способность L. reuteri DSM 17648 специфично связываться с клетками H. рylori, образуя коагрегаты, которые выводятся из организма естественным путем, в результате чего снижается уровень колонизации H. рylori в желудке [17].

Наиболее высокая эффективность и безопасность антихеликобактерной терапии отмечаются на фоне пребиотической или пробиотической терапии [18].
Применение пробиотиков предусмотрено в общепринятых клинических рекомендациях по лечению инфекции H. pylori:

В городе Екатеринбурге была проведена программа по формированию территориального регистра эрадикационной терапии H. pylori у взрослых пациентов. Показания для эрадикационной терапии у пациентов определялись в соответствии с национальными клиническими рекомендациями РГА [22].

Статистический анализ сравнения безопасности схемы терапии с L.reuteri DSM 17648 и схемы терапии без данного метабиотика продемонстрировал снижение нежелательных явлений эрадикационной терапии [22].
Частота нежелательных явлений
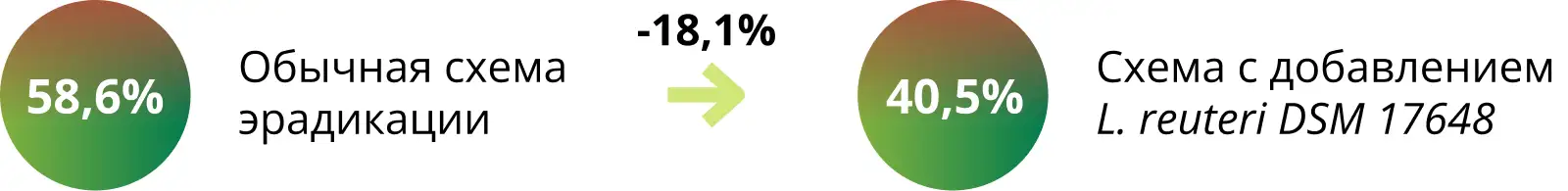
Статистический анализ сравнения эффективности схемы терапии без L. reuteri DSM 17648 и схемы терапии с данным метабиотиком продемонстрировал прирост положительных результатов эрадикации H. pylori [22] на 5,9%.
Включение в схему терапии таргетных инактивированных клеток пробиотического штамма L. reuteri DSM 17648 способствует повышению эффективности эрадикации и снижению числа побочных эффектов со стороны ЖКТ [22].

Сокращения:
ЖКТ — желудочно-кишечный тракт; РГА — российская гастроэнтерологическая ассоциация; МЗ РФ — министерство здравоохранения Российской Федерации.
Список литературы:
1. Malfertheiner, P., Schultze, V., Rosenkranz, B., Kaufmann, S. H. E., Ulrichs, T., Novicki, D., et al. (2008). Safety and immunogenicity of an intramuscular Helicobacter pylori vaccine in noninfected volunteers: a phase I study. Gastroenterology 135, 787–795. doi: 10.1053/j.gastro.2008.05.054
2. Burkitt M. D., Duckworth C. A., Williams J. M., Pritchard D. M. Helicobacter pyloriinduced gastric pathology: insights from in vivo and ex vivo models // Dis. Model. Mech. 2017. Vol. 10. 2. P. 89–104.
3. Lei Yeqing, Liu Xiaochen , Du Qin , Li Yan Bibliometric analysis of Helicobacter pylori vaccine development from 1993 to 2023 DOI=10.3389 fmicb.2025.1479195
4. Успенский Ю. П., Фоминых Ю. А., Иванов С. В., Менакер И. О. Эволюция в эрадикационнойтерапии НР-ассоциированных заболеваний. Выход за рамки стандартов. РМЖ. 2016; 17: 1144–1152.
5. Хелинорм® – актуальные возможности в профилактике и терапии инфекции Helicobacter pylori. Электронный ресурс https://umedp.ru/ articleskhelinorm_aktualnye_vozmozhnosti_v_profilaktike_i_terapii_infektsii_helicobacter_pylori_43ya_nauchna.html (дата доступа 29.09.2017 г.)
6. Бакулина Н. В. и др. Пробиотики в схемах эрадикации Helicobacter pylori: современные данные и результаты собственного исследования. Consilium Medicum. 2019; 21(8): 58-64.
7. Agarwal, Kanishtha et al. Helicobacter pylori Vaccine: From Past to Future. Mayo Clinic Proceedings, Volume 83, Issue 2, 169 – 175
8. Успенский Ю. П. и др. Вакцина против Helicobacter pylori: миф или реальность. Инфекция и иммунитет. 2019; 9(3-4):457-466.
9. Kreiss, C. et alSafety of oral immunisation with recombinant urease in patients with Helicobacter pylori infection. The Lancet, Volume 347, Issue 9015, 163 – 163.
10. Maleki Kakelar H., Barzegari A., Dehghani J., Hanifian S., Saeedi N., Barar J., Omidi Y. Pathogenicity of Helicobacter pylori in cancer development and impacts of vaccination. Gastric Cancer. 2019 Jan;22(1):23-36. doi: 10.1007/s10120-018-0867-1. Epub 2018 Aug 25. PMID: 30145749.
11. Zeng, Ming et al. Efficacy, safety, and immunogenicity of an oral recombinant Helicobacter pylori vaccine in children in China: a randomised, double-blind, placebo-controlled, phase 3 trial. The Lancet, Volume 386, Issue 10002, 1457 – 1464
12. Guo L., Zhang F., Wang S., Li R., Zhang L., Zhang Z., Yin R., Liu H., Liu K. Oral Immunization With a M Cell-Targeting Recombinant L. Lactis Vaccine LL-plSAM-FVpE Stimulate Protective Immunity Against H. Pylori in Mice. Front Immunol. 2022 Jul 7; 13:918160. doi: 10.3389/fimmu.2022.918160. PMID: 35911756; PMCID: PMC9336465.
13. Safarov T., Kiran B., Bagirova M., Allahverdiyev A. M., Abamor E. S. An overview of nanotechnology-based treatment approaches against Helicobacter Pylori. Expert Rev Anti Infect Ther. 2019 Oct;17(10):829-840. doi: 10.1080/14787210.2019.1677464. Epub 2019 Oct 16. PMID: 31591930.
14. Huang T. T., Cao Y. X., Cao L. Novel therapeutic regimens against Helicobacter pylori: an updated systematic review. Front Microbiol. 2024 Jun 7; 15:1418129. doi: 10.3389/fmicb.2024.1418129. PMID: 38912349; PMCID: PMC11190606.
15. Шапошников Л. А., Тишков В. И., Пометун А. А. Лактобактерии и клебсиеллы: две противоположности в борьбе за здоровье организма //Успехи биологической химии. 2024; 64: 143–178.
16. Захарова И. Н., Бережная И. В., Сугян Н. Г., Санникова Т. Н., Кучина А. Е., Сазанова Ю. О. Что мы знаем сегодня о Lactobacillus reuteri? МС. 2018; 2.
17. Holz C., Busjahn A., Mehling H., Arya S., Boettner M., Habibi H., Lang C. Significant Reduction in Helicobacter pylori Load in Humans with Non-viable Lactobacillus reuteri DSM17648: A Pilot Study. Probiotics Antimicrob Proteins. 2015 Jun;7(2):91-100. doi: 10.1007/s12602-014-9181-3. PMID: 25481036; PMCID: PMC4415890.
18. Лазебник Л. Б. и др. Helicobacter pylori, хеликобактериоз и ассоциированные заболевания (VIII Московские соглашения по диагностике и лечению хеликобактериоза у взрослых и детей) Руководство для врачей. Экспериментальная и клиническая гастроэнтерология. 2024; 12: 49–145.
19. Клинические рекомендации "Гастрит и дуоденит", 2024 г. МЗ РФ. Электронный ресурс https://gastroscan.ru/literature/pdf/klin-reg-gastrit-duodenit-2024.pdf (Дата доступа 01.10.2025).
20. Клинические рекомендации "Язвенная болезнь", 2024 г. МЗ РФ. Электронный ресурс https://endoexpert.ru/dokumenty-i-prikazy/yb2026/ (Дата доступа 01.10.2025).
21. Malfertheiner P., Megraud F., Rokkas T. et al. Management of Helicobacter pylori infection: the Maastricht VI/Florence consensus report. Gut. 2022; 71: 1724–1762.
22. Хлынов И. Б. и др. Роль Lactobacillus reuteri DSM 17648 в эрадикационной терапии инфекции Helicobacter pylori у взрослых в реальной клинической практике. Лечащий врач. 2020; 2: 19-22.
23. Листок-вкладыш к БАД Хелинорм®.
24. MARANON J. A., Hernández-Bueno A. Limosilactobacillus reuteri DSM 17648 in Helicobacter pylori infection: clinical information and mechanisms. American Journal of Medical and Clinical Research & Reviews. 2024; 3(4): 1–11.
Только для медицинских и фармацевтических работников. Для распространения на территории РФ в местах проведения медицинских и фармацевтических выставок, семинаров, конференций и иных подобных мероприятий и в предназначенных для медицинских и фармацевтических работников специализированных печатных изданиях.
ООО «Др. Реддис Лабораторис»,
115035, г. Москва, Овчинниковская наб., д. 20, стр. 1
Телефон: +7 (495) 783-29-01
R1381691-16092025-HCP-HEL
Комментарии (0)