Категории
Сменить пароль!
Сброс пароля!


Выдающиеся достижения в области медицины, произошедшие за последние годы, позволили перейти от универсального подхода к более индивидуальному и точному [1]. Врачи всегда стремились улучшить свои практические навыки и обеспечить большую эффективность лечения и безопасность своих пациентов, опираясь на достижения предыдущих поколений. С помощью электронных медицинских карт, суперкомпьютеров, аналитики больших массивов данных и генетического анализа (всех компонентов, необходимых для внедрения того, что быстро становится по-настоящему точной и персонализированной медициной), ученые и врачи теперь могут далеко продвинуться в этой миссии [2].
Прецизионная медицина и персонализированная медицина — два термина, популярность которых выросла в связи со сдвигом парадигмы. В медицине традиционно придерживаются универсального подхода, при котором лечение разрабатывают на основе средних показателей популяции. Однако эта стратегия не учитывает врожденных различий между пациентами. Согласно подходу прецизионной и персонализированной медицины, каждый человек генетически и биологически индивидуален, и поэтому их ответ на лечение может значительно различаться [3].
Эти подходы учитывают уникальную генетику человека, факторы окружающей среды и образа жизни, предлагая индивидуальные медицинские вмешательства [4]. Персонализированная медицина включает в себя подход к лечению пациентов, который учитывает не только их генетические характеристики, но и такие факторы, как предпочтения, убеждения, отношения, знания и социальный контекст. С другой стороны, в прецизионной медицине модель предоставления медицинской помощи в значительной степени зависит от данных, аналитики и информации для обеспечения целенаправленного и точного лечения [5].
Благодаря использованию генетических характеристик пациента у персонализированной медицины есть потенциал для обеспечения пациента индивидуально подобранными лекарственными препаратами в точных дозировках и в оптимальные сроки, что повышает эффективность медицинской практики и снижает расходы на здравоохранение [6]. В прецизионной медицине используется более тонкая стратегия, которая учитывает генотипические и фенотипические различия, чтобы создать терапевтический или профилактический метод, способный принести пользу как популяциям в целом, так и отдельным пациентам [7].
Прогресс в прецизионной медицине приводит к ощутимым преимуществам, в том числе к возможности выявлять заболевания на ранней стадии и создавать персонализированные планы лечения. Персонализированная медицинская помощь, ставшая возможной благодаря прецизионной медицине, основана на различных технологиях сбора и анализа данных. Следует отметить, что интеграция высокопроизводительного генотипирования с широким использованием электронных медицинских карт предоставляет ученым беспрецедентную возможность выделять новые фенотипы на основании данных клинической практики и данных по биомаркерам.
Эти фенотипы в сочетании с данными электронных медицинских карт могут служить обоснованием потребности в дополнительном лечении или повысить точность диагностики вариантов заболевания [8]. В этой статье рассматривается концепция прецизионной и персонализированной медицины и ее потенциал для открытия новой эры в здравоохранении.
Прецизионная медицина и персонализированная медицина: в чем отличия?
Новая эра «персонализированной» или «прецизионной» медицины, учитывающей индивидуальную генетику и другие источники изменчивости в лечении и профилактике заболеваний, началась благодаря достижениям в области геномики и других «омических» технологий [9]. Национальный исследовательский совет утверждает, что «персонализированная медицина» — это понятие, схожее по коннотации с понятием «прецизионная медицина» [10]. Понятия «прецизионная медицина» и «персонализированная медицина» обычно используются как взаимозаменяемые. Однако между этими двумя понятиями есть небольшие отличия.

(A) Прецизионная медицина. Прецизионная медицина — это подход, направленный на адаптацию лекарственных препаратов и вмешательств для определенных пациентов на основе их специфических характеристик, включая их генетический состав, факторы окружающей среды, образ жизни и другие соответствующие данные. Особое внимание уделяется индивидуализации здравоохранения для оптимизации эффективности и уменьшения побочных эффектов.
Цель этого подхода — предложить пациенту правильное лечение в нужное время. Прецизионная медицина опирается на достижения в таких технологиях, как геномика, протеомика и другие «омические» области, а также биоинформатика и анализ данных для выявления молекулярных и генетических маркеров, которые могут способствовать прогнозированию риска заболевания, диагностике и принятию решения о лечении (рисунок 1).
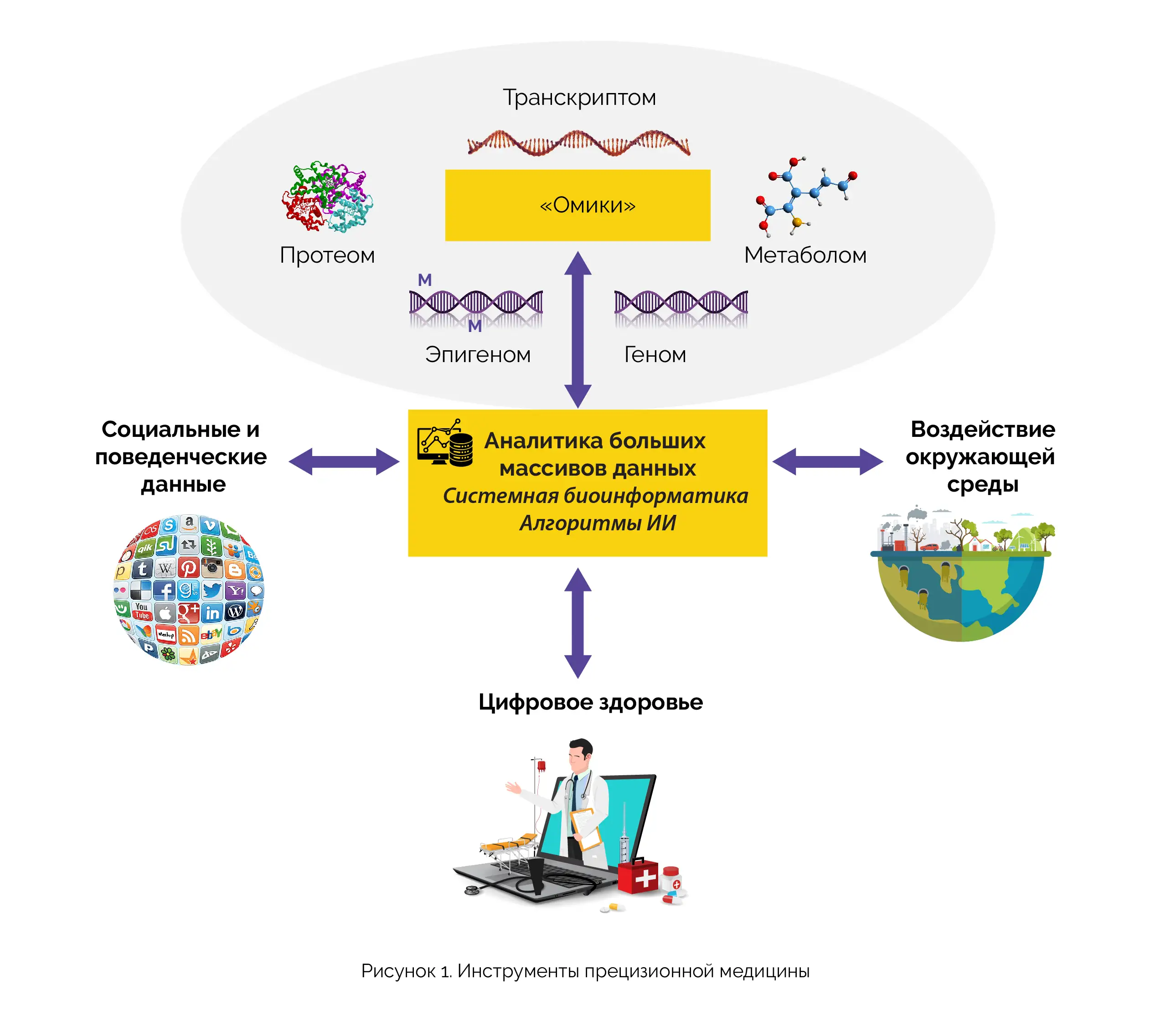
Благодаря пониманию уникальных генетических и молекулярных профилей пациентов прецизионная медицина позволяет проводить более целенаправленные и индивидуальные вмешательства.
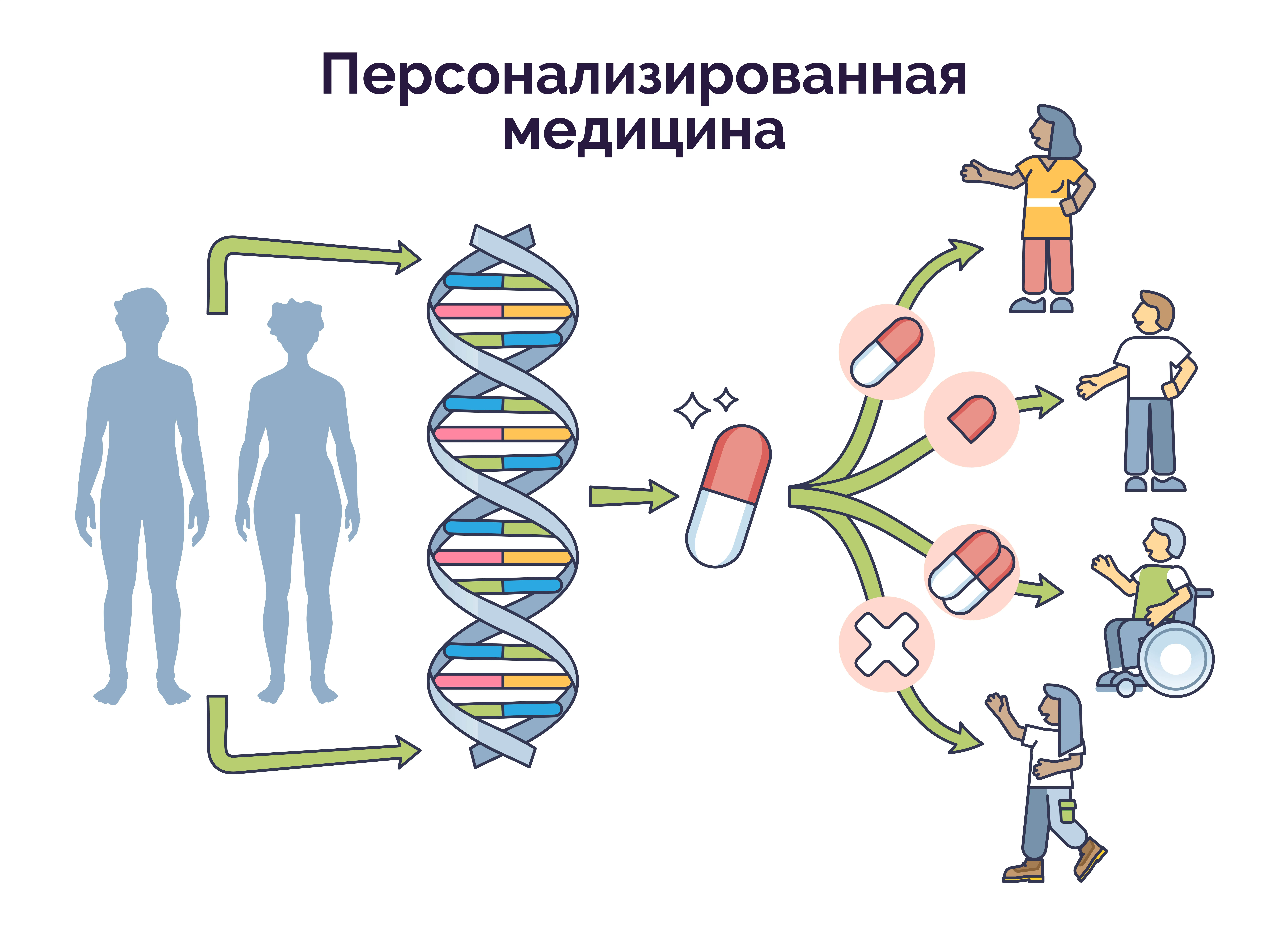
(B) Персонализированная медицина. С другой стороны, в персонализированной медицине используется более широкий подход, учитывающий не только индивидуальные биологические характеристики пациента, но и его личные предпочтения, ценности и обстоятельства. Согласно подходу персонализированной медицины, решения в области здравоохранения должны приниматься совместно с пациентами и с учетом их уникальных потребностей и обстоятельств.
Для создания комплексного плана медицинской помощи, соответствующего целям и ценностям пациента, в дополнение к биологическим факторам персонализированная медицина учитывает социальные, психологические и поведенческие аспекты. Основное внимание уделяется лечению, ориентированному на пациента, расширению прав и возможностей пациентов, а также совместному принятию решений. Прецизионная медицина фокусируется в первую очередь на биологических и молекулярных аспектах индивидуализации здравоохранения, а персонализированная медицина расширяет эту концепцию с целью создания более целостного взгляда на пациента и его путь лечения.
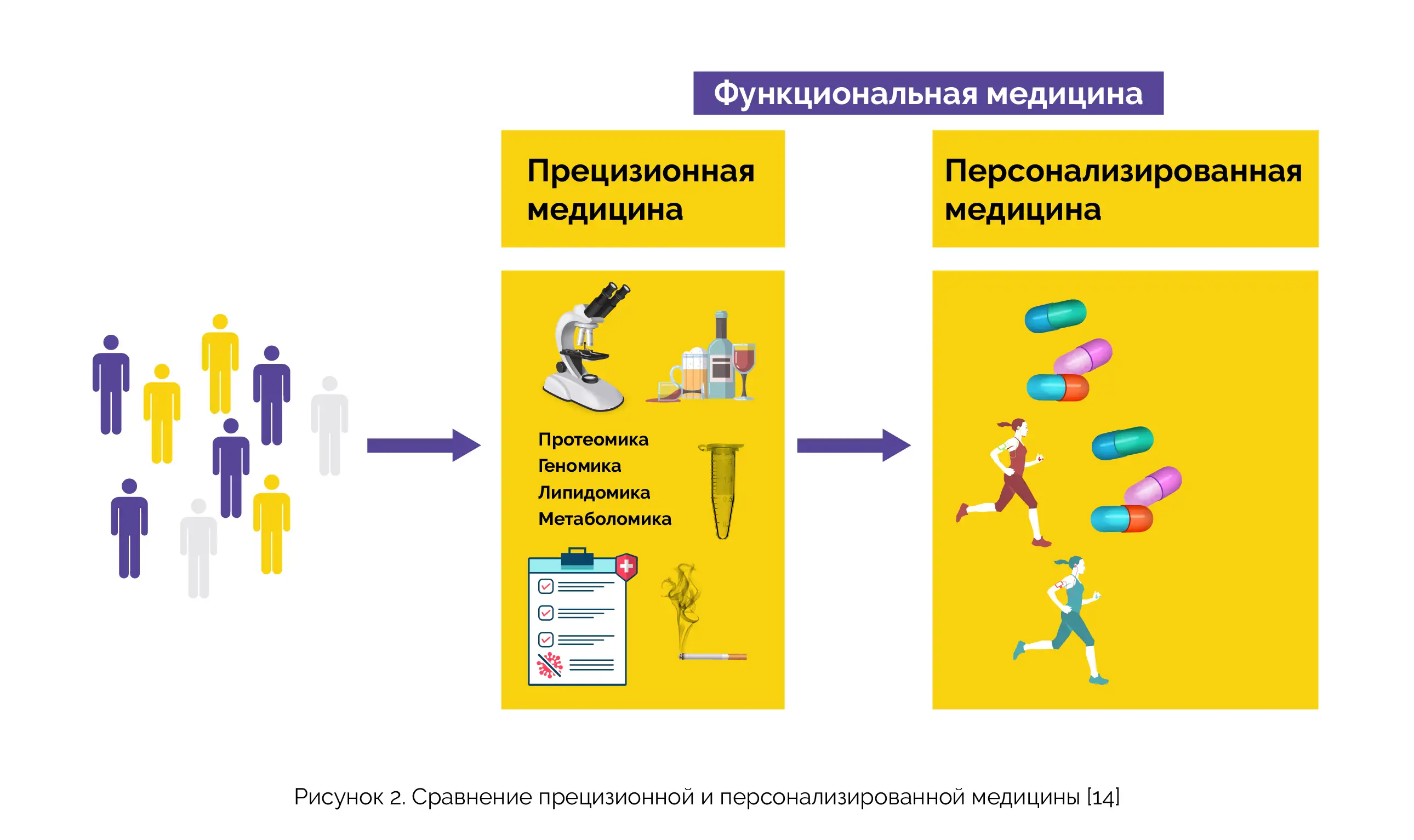
Таким образом, в прецизионной медицине особое значение придается использованию молекулярной и генетической информации для принятия решений о лечении, а в персонализированной медицине при создании индивидуального плана лечения учитывается более широкий спектр факторов, включая предпочтения и ценности пациента (рисунок 2) [11–13].
Роль прецизионной и персонализированной медицины в революцизировании здравоохранения
Важные результаты исследований в области геномики, полученные за последние несколько десятилетий, породили большие надежды на ее глубокое влияние на область биомедицины. В связи с этим значительно увеличилось финансирование исследований в области персонализированной или прецизионной медицины, направленных на адаптацию медицинских подходов к отдельным пациентам. Этот подход основан на генетическом анализе, выявлении биомаркеров и создании лекарственных препаратов направленного действия с целью предоставления индивидуальной медицинской помощи.
В последние годы прецизионная и персонализированная медицина стали революционными подходами в сфере здравоохранения [6]. Давайте рассмотрим, как прецизионный и персонализированный подходы к охране здоровья могут улучшить прогнозирование, профилактику и лечение заболеваний у отдельных лиц и их семей.

(А) Прогнозирование и профилактика
1. Понимание истории состояния здоровья семьи пациента имеет решающее значение
Информация о хронических заболеваниях, распространенных среди членов семьи пациента, включая сахарный диабет, заболевания сердца, высокое артериальное давление или онкологические заболевания, может дать представление о факторах риска этого пациента. Предоставление этой информации лечащему врачу позволяет принимать активные меры для профилактики заболеваний или их раннего выявления. В определенных случаях лечащий врач может порекомендовать генетическое консультирование и генетический анализ, чтобы оценить предрасположенность пациента к заболеваниям, распространенным в его семье.
2. Использование мобильных медицинских приложений
Использование интеллектуальных устройств и мобильных медицинских приложений позволяет отслеживать жизненно важную информацию о состоянии здоровья, такую как питание, физическая активность и артериальное давление. Измерения в режиме реального времени помогают отслеживать прогресс и получать оповещения о любых изменениях, которые могут потребовать медицинской помощи. Однако важно отметить, что эти устройства не должны заменять регулярные медицинские осмотры, а служат дополнительными инструментами.
3. Использование возможностей социальных сетей
Исследователи общественного здравоохранения изучают потенциал социальных сетей в отслеживании вспышек заболеваний. Отслеживая сообщения с информацией о симптомах, можно собрать ценную информацию для выявления и анализа тенденций. Департаменты здравоохранения могут эффективно передавать важную медицинскую информацию более широкой аудитории через платформы социальных сетей.
4. Выявление вспышек инфекционных заболеваний
Секвенирование генома играет жизненно важную роль в выявлении специфических патогенов, вызывающих заболевания, путем создания их ДНК-фингерпринтов. Эта информация позволяет врачам и представителям органов здравоохранения точно определять источники инфекций и выбирать оптимальные стратегии лечения. Становится возможным точное отслеживание патогенов, что способствует принятию эффективных мер по борьбе с заболеваниями.
5. Профилактика осложнений за счет раннего вмешательства
Скрининг новорожденных — критически важный процесс, который включает проведение младенцам анализов на наличие определенных заболеваний практически сразу после рождения. Он включает в себя анализ крови, скрининг на потерю слуха и обследования на наличие пороков сердца. Раннее выявление этих заболеваний позволяет своевременно начать лечение, снижая риск инвалидности или смерти.
6. Профилактика заболеваний у лиц с генетической предрасположенностью
Некоторые лица имеют врожденные патологические состояния, которые повышают их предрасположенность к определенным заболеваниям. Например, лица с мутациями гена BRCA1 или BRCA2 имеют более высокий риск развития рака молочной железы или яичников, а лица с синдромом Линча склонны к колоректальному и другим видам рака. Выявление этих состояний дает возможность предпринять превентивные меры, такие как более раннее или более частое обследование, применение лекарственных препаратов или даже хирургические вмешательства, чтобы снизить риск заболевания.
(B) Лечение и ведение
1. Анализ биомаркеров помогает врачам выбрать наиболее эффективное лечение
При анализе на биомаркеры, также известном как профилирование опухоли или генетическое исследование опухоли, изучают генетические или другие изменения, происходящие при солидных опухолях и при злокачественных заболеваниях крови. Выявляя такие изменения, врачи могут определить наиболее подходящий вариант лечения. Даже если у двух пациентов один и тот же тип онкологического заболевания, их лечение может отличаться. На основании результатов анализа на биомаркеры также можно спрогнозировать вероятность рецидива онкологического заболевания, помогая пациенту решить, следует ли проводить лечение, такое как химиотерапия или лучевая терапия.
2. Фармакогеномика помогает врачам назначить наиболее подходящий лекарственный препарат и дозировку
На ответ пациента на лекарственный препарат влияют различные факторы, в том числе его ДНК. У одних пациентов определенный препарат может быть эффективным, а у других тот же самый препарат может оказаться неэффективным или даже привести к развитию серьезных побочных эффектов. Фармакогеномика изучает, как ДНК пациента влияет на ответ на лекарственный препарат, и помогает врачам выбрать безопасный и эффективный для пациента лекарственный препарат и дозировку.
3. Применение систем непрерывного мониторинга уровня глюкозы позволяет улучшить дозировку инсулина
Регулярный мониторинг уровня глюкозы в крови имеет решающее значение для эффективной инсулинотерапии сахарного диабета. В системах непрерывного мониторинга глюкозы используются датчики, которые крепятся к руке или животу и обеспечивают постоянный мониторинг уровня глюкозы в крови. Их использование улучшает дозировку инсулина, предупреждает осложнения и позволяет пациенту делиться своими результатами с врачом.
4. Мобильные устройства способствуют здоровому образу жизни и улучшают лечение хронических заболеваний
Персональные устройства способны отслеживать поведение человека, в том числе физическую активность, режим питания и режим сна. Их также можно использовать для напоминания о приеме лекарственных препаратов, практиках осознанности, регулярных осмотрах и скринингах на онкозаболевание [15].
Появление прецизионной медицины создало широкие возможности для развития современного здравоохранения и придало практическое значение концепции персонализированной медицины. Прецизионная медицина кардинальным образом изменяет классификацию заболеваний, создавая персонализированную систему, которая отличается от традиционного подхода. Прецизионная медицина играет решающую роль в точной классификации и диагностике заболеваний путем интеграции клинических характеристик пациентов с разнообразными «омическими» данными.
Этот подход позволяет реализовать целевые стратегии профилактики и лечения, гарантируя, что пациенты получат соответствующие вмешательства, в дозах и в сроки, соответствующие их специфическим потребностям [16].
Давайте рассмотрим значение прецизионной и персонализированной медицины в контексте различных заболеваний.
(а) Онкологическое заболевание
Онкологи, несомненно, стали основоположниками прецизионной медицины. Переход к персонализированной терапии, вероятно, обусловлен несколькими факторами, в том числе преобладающей цитотоксичностью и значительными побочными эффектами, связанными с существующими универсальными противоопухолевыми препаратами. Кроме того, выявление специфических уязвимых мест в опухолях в качестве потенциальных терапевтических мишеней также способствует внедрению персонализированных подходов к лечению. Следует отметить, что существует два основных способа создания методов лечения для более целенаправленного воздействия на раковые клетки:
Таргетные препараты защищают здоровые клетки и способствуют стратификации типов опухолей, что позволяет индивидуализировать методы лечения в соответствии с ними [17]. У лиц, являющихся носителями определенных вариаций генов BRCA1 или BRCA2, пожизненный риск развития рака молочной железы составляет до 85 %, а рака яичников — до 60 %. Результаты генетических анализов на BRCA1 и BRCA2 могут стать ценным источником информации для составления рекомендаций по осуществлению профилактических мер, включая более частые маммографические обследования, профилактические операции и рассмотрение стратегий химиопрофилактики [18].
Иматиниб, ингибитор, который специфически нацелен на химерный ген BCR-ABL при хроническом миелогенном лейкозе и мутациях с усилением функции в генах, ответственных за рецептор фактора роста тучных/стволовых клеток (KIT) или рецептор фактора роста тромбоцитов α (PDGFRα) при желудочно-кишечных стромальных опухолях, является ранним и ярким примером успешной таргетной противораковой терапии [17].
(b) Бронхиальная астма
В области хронических воспалительных заболеваний, таких как бронхиальная астма, внедрение прецизионной медицины и персонализированной терапии представляет собой важную цель. Для достижения этого важно точно классифицировать различные подтипы бронхиальной астмы с помощью надежных диагностических критериев, включая генетические маркеры и биомаркеры [19]. Например, несмотря на резкое снижение уровня эозинофилов, было доказано, что меполизумаб (антитело к интерлейкину-5 (IL-5)) клинически неэффективен у пациентов с бронхиальной астмой среднетяжелого течения. Однако 10 лет спустя было установлено, что он очень эффективен у лиц с гиперэозинофильным синдромом.
Поскольку эозинофильный путь IL-5 не актуален для большинства астматиков, предполагалось, что его блокирование не будет иметь клинически значимого эффекта. Согласно данным исследований, для эффективности омализумаба уровень свободного иммуноглобулина Е (IgE) должен быть ниже 50 г/мл. Его дозу корректируют с учетом массы тела и исходного уровня IgE, чтобы добиться желаемого снижения уровня IgE [17].
(с) Редкие заболевания
Прецизионная медицина прокладывает путь к выявлению потенциальных методов лечения лиц с редкими заболеваниями, учитывая, что примерно 1 из 10 человек страдает одним из 10 000 редких заболеваний [20]. Лица с редкими заболеваниями часто проходят сложный путь, известный как «диагностическая одиссея». Он включает продолжительные и изнурительные циклы анализов и посещений клиник, которые в некоторых случаях могут длиться несколько лет, в надежде выявить основную причину их состояния. Для таких пациентов получение генетического диагноза знаменует окончание «диагностической одиссеи» и начало «терапевтической одиссеи» [21].
(d) Нарушения метаболизма
(i) Дислипидемия. Создание ингибиторов пропротеин конвертазы субтилизин/кексин типа 9 (PCSK9) — это яркий пример того, как молекулярные, фенотипические и генетические данные стали основанием для использования PCSK9 в качестве терапевтической мишени при гиперхолестеринемии. Научные данные подтвердили, что PCSK9, белок, секретируемый печенью, циркулирует в кровотоке и связывается с рецепторами липопротеинов низкой плотности (ЛПНП), которые играют решающую роль в выведении холестерина из кровотока. Такое связывание затем вызывает эндоцитоз рецептора ЛПНП и последующую деградацию.
За счет увеличения количества рецепторов ЛПНП, которые становятся доступными в результате ингибирования PCSK9, уровни ЛПНП-Х в плазме снижаются. После введения алирокумаба и эволокумаба наблюдалось статистически значимое снижение (36–60 %) уровня ЛПНП-Х, что привело к их одобрению Управлением по контролю качества пищевых продуктов и лекарственных средств США (FDA). Мутация потери функции гена ANGPTL4 связана со здоровым липидным профилем и снижением риска ишемической болезни сердца. Эти эффекты моноклональных антител подтверждаются на моделях животных, что усиливает аргументы в пользу ANGPTL4 как потенциальной терапевтической мишени для лечения ишемической болезни сердца [17].
(ii) Сахарный диабет.
У пациентов с сахарным диабетом методы персонализированной медицины можно использовать в разных аспектах, в том числе выявление факторов риска, распределение ресурсов, выбор индивидуальной терапии и мониторинг ответа с помощью биомаркеров. Генетические вариации, такие как однонуклеотидные полиморфизмы (ОНП) в таких генах, как ABCC8, SLC22A1, SLC22A2 и PPARG, влияют на ответ на пероральные противодиабетические препараты. У пациентов с сахарным диабетом персонализированная медицина выходит за рамки лечения клинических и лабораторных отклонений и учитывает психологическое и социальное благополучие пациентов.
Кроме того, интеграция инициатив цифрового здравоохранения и вычислительных платформ с «омическими» данными (геномика, протеомика, метаболомика и транскриптомика) произвела революцию в персонализированной медицине при лечении сахарного диабета. Это позволяет более точно назначать лекарственные препараты, сводя к минимуму необходимость проб и ошибок и сокращая время, затрачиваемое на неэффективные ответы или устранение нежелательных явлений [22].
(e) Нейродегенеративное расстройство
В области неврологии прецизионная медицина может предложить варианты скрининга, внедрение методов своевременного обнаружения и диагностики, а также индивидуализацию планов лечения на основе уникальных клинических, генетических, биологических особенностей и факторов риска [23]. Благодаря разработке персонализированных методов лечения, ориентированных на определенного пациента, средств диагностики нового поколения, методов нейровизуализации и новых моделей нейродегенеративных заболеваний станет возможной эффективная терапия таких нейродегенеративных расстройств, как боковой амиотрофический склероз, лобно-височная деменция, болезнь Гентингтона, болезнь Паркинсона и болезнь Альцгеймера [24].
(f) COVID-19
Пандемия COVID-19 дает уникальную возможность использовать преимущества персонализированной медицины для решения новой проблемы общественного здравоохранения, включая профилактику, диагностику, лечение, эпиднадзор и общий контроль [25]. При неограниченных ресурсах стратегия прецизионной медицины должна начинаться с изучения геномов большой группы лиц, которые уже подверглись воздействию SARS-CoV-2, но не имеют симптомов, а также аналогичного размера группы лиц с известными факторами риска, которые либо умирают от болезни, либо находятся в критическом состоянии [26].
Персонализированная медицина может сыграть ключевую роль в понимании индивидуальной предрасположенности к инфекции и вариабельности клинических исходов, прогноза и ответа на лечение. Внедрение персонализированной медицины в клиническую практику обладает огромным потенциалом для преобразования здравоохранения за счет облегчения создания профилактических и терапевтических подходов, специально адаптированных к индивидуальным профилям. Этот подход может улучшить обнаружение вспышек и выявление паттернов передачи на локальном уровне.
Сочетание секвенирования генома SARS-CoV2 и оценки конкретных генетических вариантов у пациентов может дать ценную информацию для принятия клинических решений и улучшения борьбы со вспышкой. Кроме того, это может способствовать эффективной стратификации и отбору пациентов для клинических исследований, тем самым повышая шансы на получение положительных результатов [25].
Преимущества и проблемы
Прецизионная и персонализированная медицина обладают преобразующим потенциалом в здравоохранении, но они также характеризуются рядом преимуществ и проблем, которые необходимо осознать и решить.
Преимущества
1. Целенаправленное лечение. Одним из ключевых преимуществ прецизионной медицины и персонализированной медицины является возможность проводить целенаправленное лечение на основе специфического генетического или молекулярного профиля пациента. Этот подход позволяет проводить более эффективное лечение с более низкой частотой побочных эффектов, поскольку препараты подбираются с учетом специфических характеристик заболевания пациента.
2. Улучшенная диагностика. В прецизионной медицине и персонализированной медицине используются передовые диагностические инструменты и методы для выявления заболеваний на ранней стадии и с большей точностью. Эта ранняя и точная диагностика может способствовать своевременному проведению вмешательств, что повышает шансы на успешные исходы.
3. Прогностическая оценка риска. Анализируя генетические данные человека и данные об окружающей среде, прецизионная и персонализированная медицина может помочь оценить риск развития определенных заболеваний у человека. Эти знания позволяют принимать упреждающие меры, такие как изменение образа жизни или профилактические вмешательства, чтобы смягчить или отсрочить начало заболевания.
4. Интенсификация разработки лекарственных препаратов. Эти подходы облегчают выявление специфических молекулярных мишеней для разработки препаратов, способствуя разработке более эффективных лекарственных средств. Понимая основные механизмы заболеваний на молекулярном уровне, исследователи могут разрабатывать лекарственные препараты, которые избирательно воздействуют на болезнетворные факторы, улучшая исходы лечения.
5. Вовлечение пациентов и расширение прав и возможностей. Прецизионная медицина и персонализированная медицина расширяют возможности пациентов, вовлекая их в принятие собственных решений о лечении. Понимая свои уникальные генетические факторы и факторы окружающей среды, пациенты могут активно участвовать в планировании лечения и делать осознанный выбор в отношении своего медицинского обслуживания [12, 13, 27].
Проблемы
Хотя ожидается, что персонализированная и прецизионная медицина приведет к прогрессу во многих областях здравоохранения, все еще существует множество препятствий, мешающих ее применению в клинической практике [6].
1. Интеграция данных и конфиденциальность. Успешное внедрение прецизионной медицины и персонализированной медицины зависит от интеграции и анализа больших объемов данных пациентов, включая генетическую, клиническую информацию и информацию об образе жизни. Обеспечение конфиденциальности и безопасности данных при одновременном обеспечении эффективного обмена данными и их анализа сопряжено со значительными трудностями [28].
2. Стоимость и доступность. Внедрение подходов прецизионной медицины и персонализированной медицины может быть дорогостоящим, особенно если учитывать необходимость расширенного геномного анализа, анализа данных и индивидуальных вариантов лечения. Экономическая эффективность и доступность этих подходов должны быть тщательно оценены, чтобы обеспечить равный доступ к персонализированному медицинскому обслуживанию [29].
3. Этические и юридические соображения. Использование генетической и молекулярной информации в прецизионной медицине вызывает этические и юридические вопросы, такие как конфиденциальность, согласие и потенциальная дискриминация на основе генетических характеристик. Для решения этих проблем и защиты прав пациентов необходимо разработать и принять соответствующие руководства и нормативно-правовые акты [30].
4. Ограниченная доказательная база. Хотя прецизионная медицина и персонализированная медицина открывают большие перспективы, доказательная база их эффективности при различных заболеваниях все еще находится в процессе развития. Необходимы дальнейшие научные и клинические исследования, чтобы установить обоснованность и эффективность этих подходов в различных группах населения и при разных заболеваниях [31].
5. Проблемы внедрения. Интеграция прецизионной медицины и персонализированной медицины в рутинную клиническую практику требует значительных изменений в системе оказания медицинской помощи, включая обучение медицинских работников, разработку соответствующей инфраструктуры и внедрение новых технологий. Преодоление этих проблем реализации необходимо для широкого внедрения и успешной интеграции этих подходов [32].
Главные тезисы
Прошли времена универсальных методов лечения; вместо этого у врачей в настоящее время появились инструменты и знания для адаптации медицинских вмешательств для определенных пациентов с учетом их уникальных характеристик и потребностей. Этот сдвиг парадигмы открыл целый мир возможностей, позволяя проводить более точную диагностику, целенаправленную терапию, улучшая исходы лечения пациентов [6]. Прецизионная и персонализированная медицина в последнее время приобрела растущую популярность в различных научных дисциплинах, и, вероятно, в ближайшие годы они приобретут еще большее значение [10].
По мере продолжения их развития это приближает нас к будущему здравоохранения, которое будет адаптировано к каждому отдельному пациенту, предлагая более точные, предсказуемые и эффективные варианты лечения. Растущие знания о генетике и геномике, а также их влиянии на здоровье, заболевание и ответ на лекарственные препараты позволяют врачам повышать эффективность профилактики заболеваний, ставить более точные диагнозы, назначать более безопасные лекарственные препараты и более эффективные методы лечения широкого спектра заболеваний, влияющих на благополучие населения [33].
Развитие высокопроизводительных технологий и разработка биологических систем могут объяснить значительный интерес к этой области. Успехи в интерпретации и использовании генетических данных будут способствовать более глубокому пониманию физиологических процессов как в здоровом состоянии, так и в активной фазе заболевания. Эти углубленные знания будут способствовать персонализации подходов к лечению и диагностике. Кроме того, в персонализированной медицине существует тенденция к экономии расходов на здравоохранение и профилактике побочных эффектов благодаря более простому выбору подходящего лекарственного препарата в нужное время для определенного пациента. Однако персонализированный подход нельзя применять ко всем заболеваниям.
При принятии решений по различным заболеваниям необходимо интегрировать небиологические, биологические аспекты и аспекты окружающей среды. Кроме того, по-прежнему необходимо оценивать важность каждой персонализированной стратегии лечения. Чтобы подтвердить эффективность любого предложенного персонализированного подхода, необходимо провести клинические исследования, которые могут предоставить доказательства его большей эффективности по сравнению с существующими методами лечения, основанными на рекомендациях [10].
В заключение следует отметить, что прецизионная медицина и персонализированная медицина обладают преобразующим потенциалом в здравоохранении. Используя индивидуальную изменчивость и адаптируя вмешательства к специфическим потребностям пациентов, эти подходы обеспечивают более точную диагностику, целенаправленную терапию и улучшение результатов лечения пациентов. Их интеграция в рутинную клиническую практику может произвести революцию в оказании медицинской помощи и улучшить здоровье населения [34].
Список литературы
1. Stefanicka-Wojtas D, Kurpas D. Personalised Medicine-Implementation to the Healthcare System in Europe (Focus Group Discussions). Journal of Personalized Medicine. 2023 Feb 21;13(3):380.
2. What Are Precision Medicine and Personalized Medicine?
Доступно по ссылке: https://healthitanalytics.com/features/what-are-precision-medicine-and-personalized-medicine (дата последнего обращения: 31 мая 2023 г.)
3. Is Personalized Medicine the Future of Healthcare? Доступно по ссылке: https://www.news-medical.net/health/Is-Personalized-Medicine-the-Future-of-Healthcare.aspx (дата последнего обращения: 31 мая 2023 г.)
4. Prosperi M, Min JS, Bian J, Modave F. Big data hurdles in precision medicine and precision public health. BMC Medical Informatics and Decision Making. 2018 Dec 29;18(1):139.
5. Ginsburg GS, Phillips KA. Precision Medicine: From Science To Value. Health Affairs (Millwood). 2018 May;37(5):694-701.
6. Iriart JA. Precision medicine/personalized medicine: a critical analysis of movements in the transformation of biomedicine in the early 21st century. Cadernos de Saúde Pública. 2019 Mar 25;35.
7. Precision vs. Personalized Medicine. Доступно по ссылке: https://www.news-medical.net/health/Precision-vs-Personalized-Medicine.aspx (дата последнего обращения: 31 мая 2023 г.)
8. Johnson KB, Wei WQ, Weeraratne D, Frisse ME, Misulis K, Rhee K, Zhao J, Snowdon JL. Precision Medicine, AI, and the Future of Personalized Health Care. Clinical and Translational Science. 2021 Jan;14(1):86-93.
9. The Shift From Personalized Medicine to Precision Medicine and Precision Public Health: Words Matter! Доступно по ссылке: https://blogs.cdc.gov/genomics/2016/04/21/shift/
(дата последнего обращения: 31 мая 2023 г.)
10. Strianese O, Rizzo F, Ciccarelli M, Galasso G, D’Agostino Y, Salvati A et al. Precision and personalized medicine: how genomic approach improves the management of cardiovascular and neurodegenerative disease. Genes. 2020 Jul 6;11(7):747.
11. Naithani N, Sinha S, Misra P, Vasudevan B, Sahu R. Precision medicine: Concept and tools. Medical Journal Armed Forces India. 2021 Jul;77(3):249-257.
12. National Research Council (US) Committee on A Framework for Developing a New Taxonomy of Disease. Toward Precision Medicine: Building a Knowledge Network for Biomedical Research and a New Taxonomy of Disease. Washington (DC): National Academies Press (US); 2011.Доступно по ссылке: https://www.ncbi. Идент. номер на книжной полке: NBK91503, PMID: 22536618.
13. Collins FS, Varmus H. A new initiative on precision medicine. The New England Journal of Medicine. 2015 Feb 26;372(9):793-5.
14. Carbonara K, MacNeil AJ, O’Leary DD, Coorssen JR. Profit versus Quality: The Enigma of Scientific Wellness. Journal of Personalized Medicine. 2022 Jan 3;12(1):34.
15. Precision health: Improving health for each of us and all of us. Доступно по ссылке: https://www.cdc.gov/genomics/about/precision_med.htm#:~:text=Precision%20medicine%2C%20also%20called%20personalized,will%20work%20best%20for%20you. (Дата последнего обращения: 30 мая 2023 г.)
16. Yuan B. What Personalized Medicine Humans Need and Way to It --also on the Practical Significance and Scientific Limitations of Precision Medicine. Pharmacogenomics and Personalized Medicine. 2022 Nov 2;15:927-942.
17. Akhoon N. Precision medicine: a new paradigm in therapeutics. International Journal of Preventive Medicine. 2021;12.
18. 5 Benefits of Precision Medicine. Доступно по ссылке: https://www.reprocell.com/blog/5-benefits-of-pm (дата последнего обращения: 30 мая 2023 г.)
19. Roth M, Stolz D. Biomarkers and personalised medicine for asthma. European Respiratory Journal. 2019 Jan 1;53(1).
20. Might M, Crouse AB. Why rare disease needs precision medicine-and precision medicine needs rare disease. Cell Reports Medicine. 2022 Feb 15;3(2):100530.
21. Villalón-García I, Álvarez-Córdoba M, Suárez-Rivero JM, Povea-Cabello S, Talaverón-Rey M, Suárez-Carrillo A et al. Precision medicine in rare diseases. Diseases. 2020 Nov 13;8(4):42.
22. Mohan V, Das AK, Mukherjee JJ, Seshadri K, Sujeet J, Sanjay K. From Individualized to personalized medicine in diabetes: an expert overview. Journal of the Association of the Physicians of India. 2019:78.
23. Hampel H, Gao P, Cummings J, Toschi N, Thompson PM, Hu Y et al. The foundation and architecture of precision medicine in neurology and psychiatry. Trends in Neurosciences. 2023 Jan 13.
24. Raikwar SP, Kikkeri NS, Sakuru R, Saeed D, Zahoor H, Premkumar K et al. Next generation precision medicine: CRISPR-mediated genome editing for the treatment of neurodegenerative disorders. Journal of Neuroimmune Pharmacology. 2019 Dec;14(4):608-41.
25. Dopazo J, Maya-Miles D, García F, Lorusso N, Calleja MÁ, Pareja MJ et al. Implementing Personalized Medicine in COVID-19 in Andalusia: An Opportunity to Transform the Healthcare System. Journal of Personalized Medicine. 2021 May 26;11(6):475.
26. How to use precision medicine to personalize COVID-19 treatment according to the patient’s genes. Доступно по ссылке: https://theconversation.com/how-to-use-precision-medicine-to-personalize-covid-19-treatment-according-to-the-patients-genes-142142 (дата последнего обращения: 30 мая 2023 г.)
27. Ashley EA. The precision medicine initiative: a new national effort. JAMA. 2015 Jun 2;313(21):2119-20.
28. Hassan M, Awan FM, Naz A, deAndrés-Galiana EJ, Alvarez O, Cernea A et al. Innovations in Genomics and Big Data Analytics for Personalized Medicine and Health Care: A Review. The International Journal of Molecular Sciences. 2022 Apr 22;23(9):4645
Will Personalized Medicine Mean Higher Costs for Consumers? Доступно по ссылке: https://hbr.org/2018/03/will-personalized-medicine-mean-higher-costs-for-consumers (дата последнего обращения: 30 мая 2023 г.)
30. Cordeiro JV. Ethical and legal challenges of personalized medicine: paradigmatic examples of research, prevention, diagnosis and treatment. Revista Portuguesa de Saúde Pública. 2014 Jul 1;32(2):164-80.
31. Beckmann JS, Lew D. Reconciling evidence-based medicine and precision medicine in the era of big data: challenges and opportunities. Genome medicine. 2016 Dec;8:1-1.
32. Naithani N, Atal AT, Tilak TVSVGK, Vasudevan B, Misra P, Sinha S. Precision medicine: Uses and challenges. Medical Journal Armed Forces India. 2021 Jul;77(3):258-265.
33. WHAT IS PERSONALIZED MEDICINE? Доступно по ссылке: https://www.jax.org/personalized-medicine/precision-medicine-and-you/what-is-precision-medicine#:~:text=Tailoring%20health%20care%20to%20each,personalized%20medicine%20or%20genomic%20medicine.
(дата последнего обращения: 31 мая 2023 г.)
34. Mathur S, Sutton J. Personalized medicine could transform healthcare. Biomedical Reports. 2017 Jul;7(1):3-5.
Комментарии (1)