Категории
Сменить пароль!
Сброс пароля!


Борьба с пандемией коронавируса является непростой задачей из-за высокой частоты передачи вируса от бессимптомных носителей, появления нескольких вызывающих опасения штаммов SARS-CoV-2 и значительной вариабельности инкубационного периода (от 2 до 14 дней).
У лиц с положительным результатом теста COVID-19 без выраженных симптомов заболевания, проживающих с инфицированным лицом, при применении комбинации имдевимаба и казиривимаба отмечалось статистически значимое снижение частоты развития симптомов COVID-19 в течение 28 дней по сравнению с плацебо.
Борьба с пандемией коронавируса является непростой задачей из-за высокой частоты передачи вируса от бессимптомных носителей, появления нескольких вызывающих опасения штаммов SARS-CoV-2 и значительной вариабельности инкубационного периода (от 2 до 14 дней). В связи с наличием штаммов, не распознаваемых иммунной системой, недостаточным иммунным ответом на вакцинацию в определенных группах риска и ограниченным применением вакцин в некоторых районах по-прежнему существует риск заражения, перехода инфекции в тяжелую форму и развития долгосрочных последствий (несмотря на наличие эффективных вакцин).
У невакцинированных лиц требуется использование комплементарных методов лечения, таких как терапия моноклональными антителами к SARS-CoV-2. Моноклональные антитела с человеческой последовательностью, такие как казиривимаб и имдевимаб, блокируют проникновение вируса путем связывания с неперекрывающимися эпитопами рецепторсвязывающего домена спайк-белка SARS-CoV-2. Терапия комбинацией казиривимаба и имдевимаба снижает риск появления новых штаммов коронавируса.
Кроме того, согласно результатам исследований в условиях in vitro, сохраняется нейтрализующая активность в отношении уже существующих вызывающих озабоченность штаммов, включая штаммы дельта (B.1.617.2), альфа (B.1.1.7), гамма (P.1) и бета (B.1.351). Терапия комбинацией казиривимаба и имдевимаба эффективна для профилактики инфицирования при тесном контакте с носителем вируса, а также для лечения амбулаторных пациентов с COVID-19. В настоящее время в США получено разрешение на экстренное применение этой комбинации для лечения коронавирусной инфекции легкой и средней степени тяжести и для профилактики инфицирования после контакта с несколькими носителями вируса.
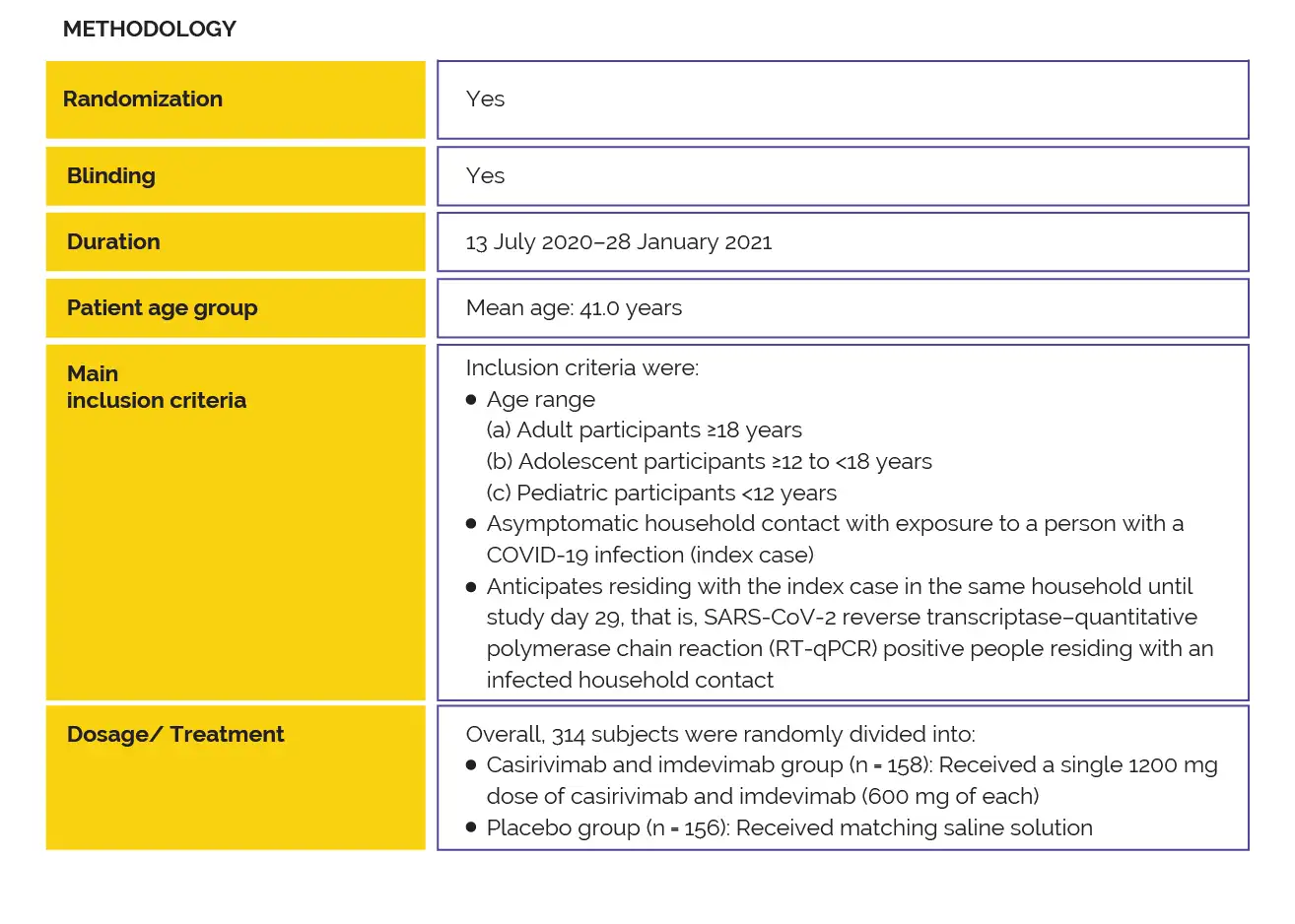
Было проведено рандомизированное клиническое исследование III фазы в двух частях с целью определения того, позволяет ли терапия казиривимабом и имдевимабом при подкожном введении в дозе 1200 мг (по 600 мг каждого антитела) предупредить инфицирование коронавирусом в условиях высокого риска при проживании с носителями вируса. Согласно результатам первой части исследования, у неинфицированных лиц, которые находятся в контакте с инфицированными, применение казиривимаба и имдевимаба способствовало статистически значимому снижению частоты развития симптоматического течения коронавирусной инфекции по сравнению с плацебо (снижение риска на 81,4 %).
В этом отчете представлены результаты части В, в которой инфицированным лицам и бессимптомным носителям, находящимся в контакте с ними, подкожно вводили комбинацию имдевимаба и казиривимаба в общей дозе 1200 мг.
ОБОСНОВАНИЕ ИССЛЕДОВАНИЯ
Ни в одном из предыдущих исследований не оценивали влияние применения казиривимаба и имдевимаба при подкожном введении у лиц с бессимптомным течением, находящихся в тесном контакте с носителями инфекции, вызванной коронавирусом SARS-CoV-2. В связи с этим было проведено настоящее рандомизированное двойное слепое плацебо-контролируемое исследование.
ЦЕЛЬ
Цель клинического исследования III фазы состояла в оценке эффективности подкожного введения комбинации казиривимаба и имдевимаба для профилактики перехода от бессимптомной формы коронавирусной инфекции к симптоматической у лиц с бессимптомным течением инфекции, которые находятся в тесном контакте с носителями вируса.
Конечные точки исследования
Результаты
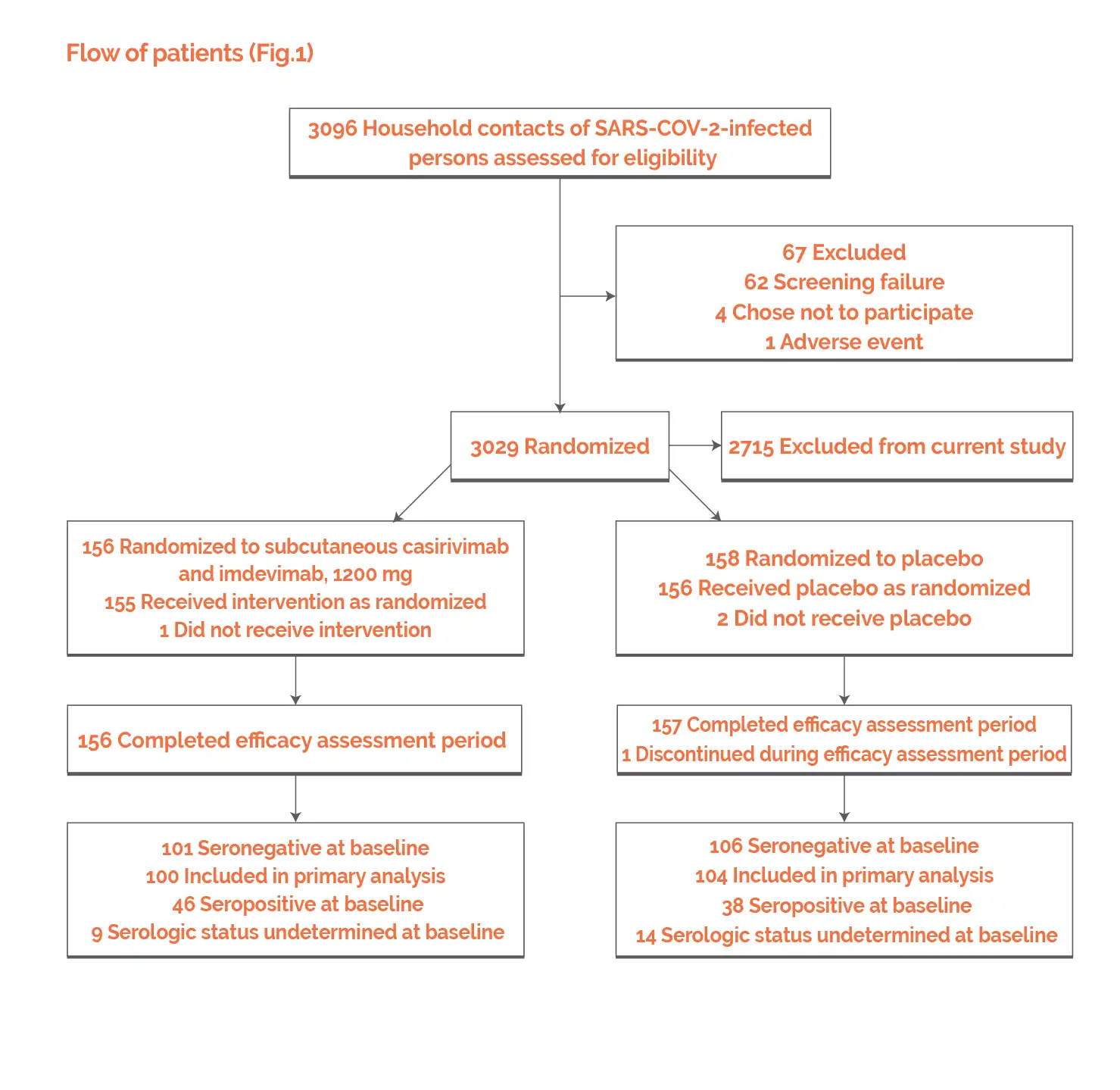
Исходный уровень: на исходном уровне статистически значимых различий между группами не выявлено.
Конечные точки исследования
Результаты
Исходный уровень: на исходном уровне статистически значимых различий между группами не выявлено.
Конечные точки исследования
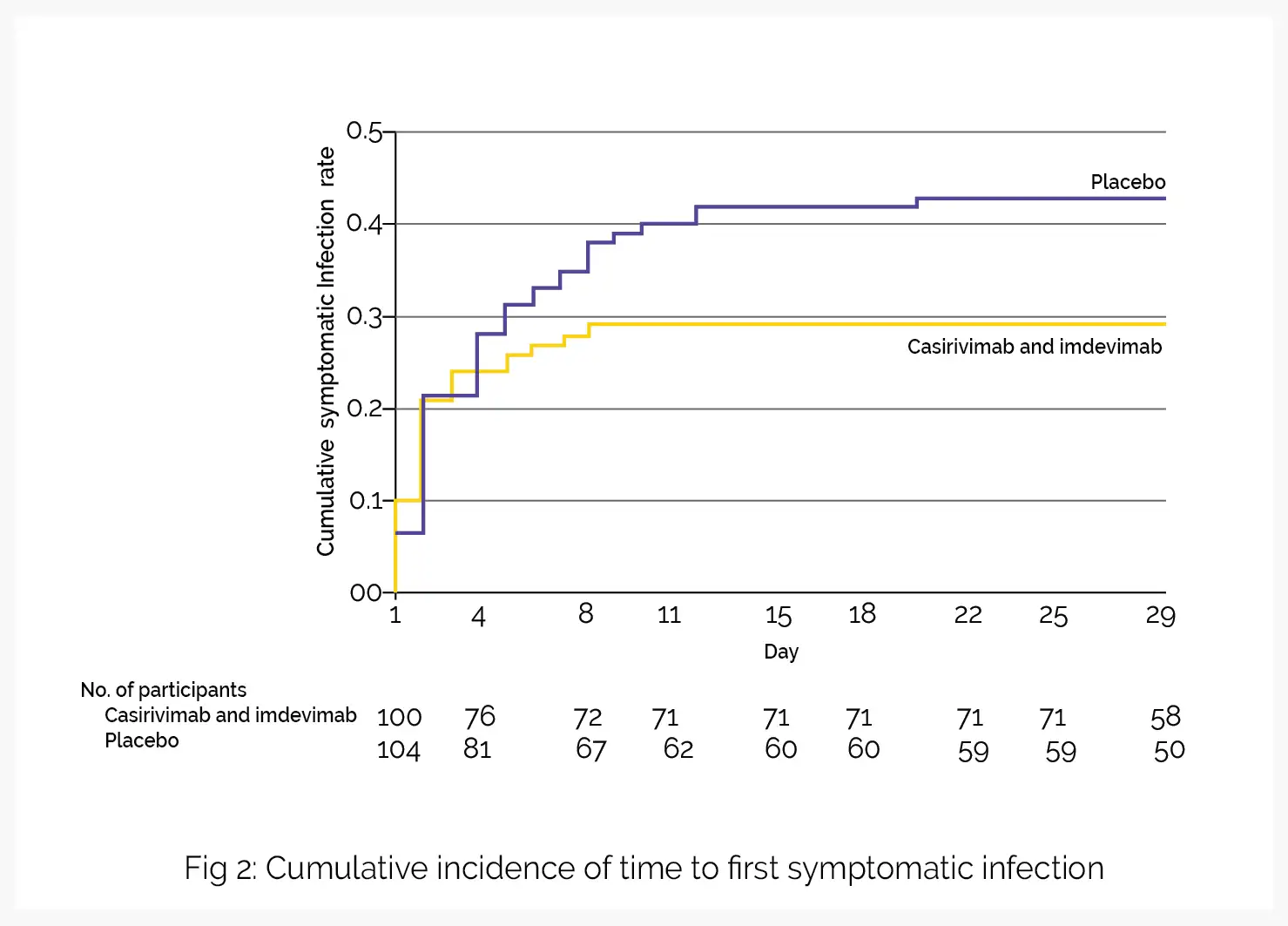
В части А исследования подкожное введение имдевимаба и казиривимаба способствовало профилактике инфицирования коронавирусом (с бессимптомным и симптоматическим течением) у неинфицированных лиц, проживающих с инфицированными. В части В исследования изучали влияние применения комбинации казиривимаба и имдевимаба у лиц с бессимптомным течением коронавирусной инфекции на раннем этапе в аналогичных условиях тесного контакта. Терапия казиривимабом и имдевимабом позволила снизить частоту развития симптомов у инфицированных лиц по сравнению с плацебо в течение 28 дней.
Результаты оценки дополнительных конечных точек свидетельствуют в пользу комбинации казиривимаба и имдевимаба по сравнению с плацебо в отношении продолжительности симптомов и обнаружения вируса в носоглотке методом ОТ-кПЦР, а также доли госпитализированных или обратившихся в отделение неотложной помощи по поводу COVID-19. Как отмечалось, снижение частоты развития симптомов и другие результаты указывают на потенциальную возможность использования моноклональных антител для лечения коронавирусной инфекции на раннем этапе.
Результаты вторичного анализа, в рамках которого оценивали основную конечную точку (развитие симптомов после бессимптомного течения инфекции), свидетельствуют об эффективности применения казиривимаба в сочетании с имдевимабом с точки зрения снижения частоты перехода течения COVID-19 в симптоматическое (начало симптоматического течения отмечалось через 3 и больше дней после завершения терапии). Однако полученные результаты являются гипотезообразующими. В ходе предварительного анализа проводили оценку основной конечной точки у всех пациентов, независимо от исходного серологического статуса.
Результаты этого анализа указывают на то, что применение комбинации казиривимаба и имдевимаба в общей популяции независимо от серологического статуса снижало вероятность перехода течения COVID-19 в симптоматическое. Для принятия решения по профилактике заражения инфекцией, вызванной коронавирусом SARS-CoV-2, у лиц после контакта с носителем вируса проведение серологического анализа в месте оказания медицинской помощи может иметь ограниченную полезность. Согласно результатам исследования III фазы с участием лиц с COVID-19, внутривенное введение казиривимаба и имдевимаба (в общей дозе 1200 мг) снижает риск смертельного исхода или госпитализации, связанных с коронавирусом, сокращает время до разрешения симптомов и быстрее снижает вирусную нагрузку по сравнению с плацебо.
Разрешение на экстренное применение допускает подкожное введение указанной комбинации в общей дозе 1200 мг в качестве альтернативного способа введения, если внутривенная инфузия невозможна и может вызвать задержку терапии. Согласно данным анализа дополнительных конечных точек в рамках текущего исследования (частота визитов к врачу в связи с коронавирусной инфекцией в течение 28-дневного периода оценки эффективности), 6 пациентов, получавших плацебо, обратились в отделение неотложной помощи или были госпитализированы, тогда как у пациентов, получавших имдевимаб и казиривимаб подкожно, данных случаев не было зарегистрировано. Это указывает на эффективность подкожного введения указанной комбинации в общей дозе 1200 мг у пациентов с COVID-19 в качестве альтернативного способа, который зарегистрирован в соответствии с действующим разрешением на экстренное применение.
В исследованиях по оценке применения имдевимаба и казиривимаба у более высокой доли лиц, получавших плацебо, отмечались одно или несколько нежелательных явлений, возникших в ходе лечения (НЯВХЛ), при этом различие объясняется увеличением числа явлений, связанных с SARS-CoV-2 в данной группе. После подкожного введения концентрация каждого антитела в сыворотке крови на 1-й день после введения дозы и в течение периода оценки эффективности продолжительностью 28 дней превышала ожидаемую целевую концентрацию, необходимую для нейтрализации, которая была определена на основании данных доклинических исследований и исследований в условиях in vitro.
Результаты анализа фармакокинетических профилей после подкожного или внутривенного введения однократных доз имдевимаба и казиривимаба указывают, что, хотя после внутривенного введения казиривимаба (600 мг) и имдевимаба (600 мг) на ранних этапах достигались высокие концентрации препаратов, при подкожном введении казиривимаба (600 мг) и имдевимаба (600 мг) через 1 день достигались средние концентрации в сыворотке крови 22,1 и 25,8 мг/л соответственно. Эти уровни, наблюдаемые в 1-й день, превышают расчетную целевую дозу, необходимую для нейтрализации вируса (20 мг/л).
Применение комбинации казиривимаба и имдевимаба позволяло предупредить переход течения COVID-19 в симптоматическое на раннем этапе у лиц с положительным результатом теста на коронавирус без симптомов заболевания (статус которых подтвержден результатом анализа методом ОТ-кПЦР), находящихся в тесном контакте с инфицированным лицом.
Таким образом, эти простые в применении методы лечения можно использовать для снижения частоты передачи вируса и предупреждения перехода бессимптомного течения инфекции в симптоматическое.
The Journal of the American Medical Association
Effect of Subcutaneous Casirivimab and Imdevimab Antibody Combination vs Placebo on Development of Symptomatic COVID-19 in Early Asymptomatic SARS-CoV-2 Infection: A Randomized Clinical Trial
Meagan P O'Brien и соавт.
Комментарии (0)